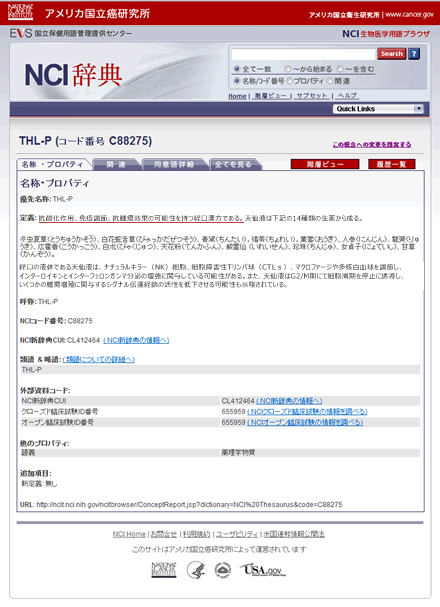
evidence 研究・試験
[結果]
全体の66.7%(治療組30人)の対象者が効果を実感し、継続服用を希望した
全体の80%の対象者が効果を実感できた
国立台湾大学医学院付属医院におけるTHL-P「天仙液」のヒト臨床試験の結果報告
国立台湾大学医学院付属医院※において、抗がん漢方薬THL-P「天仙液」による入院中の転移性乳がん(末期乳がん)患者44人を対象とした臨床試験が行われました。
なお、漢方薬による臨床試験は、付属医院設立約120年の歴史で初めてということです。
この臨床試験は、同大学付属病院、乳房腫瘍外科主治医の郭文宏医師を中心として、生薬成分の抗がん作用を含む薬理作用の結果をベースとして、その生薬を配合、処方した抗がん漢方薬THL-P「天仙液」の抗がん作用に関するエビデンス(科学的根拠)を検証したものです。

THL-P「天仙液」の臨床試験報告
①試験課題
THL-P[天仙液]の転移性乳がんに対する安全性及び有効性に関する研究
②試験目的
臨床試験による新薬の臨床研究
③試験機関
国立台湾大学医学院付属医院

④研究者
張金堅教授:元中華民国癌症医学会理事長、財団法人乳癌防治基金会取締役
郭文宏医師:国立台湾大学医学院付属医院・乳房腫瘍外科主治医師
桃建安医師:国立台湾大学医学院付属医院・家庭科主任医師
林枝輝薬剤師:漢方薬によるエイズ治療臨床試験に参加。アメリカFDA・phaseⅢ 心臓薬品開発者
⑤試験特徴
国立台湾大学医学院付属医院の設立120年以上の歴史の中で、初めてがん患者を対象とした漢方薬によるがん治療の臨床試験。
⑥試験対象者の基準
乳がん及び臨床で症状の悪化が確認され、以下の条件を満たした転移者。
A. 化学治療、放射線治療また外科手術を受けたが、効果は見られない
B. これ以上標準治療(化学治療、放射線治療また外科手術)を受けたくない
C. 余命が最低4週間以上あるとみられる
⑦試験方法
THL-P[天仙液]を服用するグループとプラシーボ(疑似薬)を服用する2つのグループに分けられました。試験方法はアメリカFDA基準である二重盲検法(実施している薬や治療法などの性質を、医師、観察者からも患者からも不明にして行う方法)が採用された。なお、グループの分け方は、くじ引きによるランダム方式で行われた。
⑧試験参加者の内訳
合計44名の内(治療組:30人 対照組:14人)
39名が骨に転移、19名が肝臓、18名が肺、4名が脳に転移していた。
⑨有効性の評価基準
1. 主要基準:QOL「生活の質」(身体機能・症状・シングルスケール)
2. 次の基準:血液生化学検査(免疫機能変化)
3. 腫瘍変化(大きさなど)
6ヶ月に及んだ臨床試験の結果
QOL(生活の質)
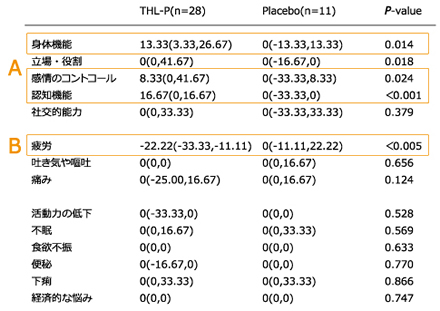
身体機能、感情のコントロール、認知性などが、天仙液服用グループはプラスの数値になっており、生活の質(QOL)が改善されています。けれども、プラシーボのグループは0で改善されていないことが分かります(A参照)。また、疲労が軽減されることから生活の質(QOL)の改善に関して、信頼性があるということを示しています(B参照)。
血液生化学検査
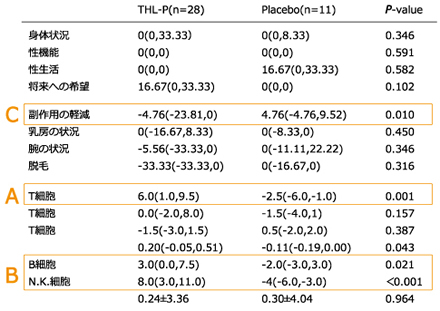
免疫機能に関して、天仙液服用グループのキラーT細胞の数値が6.0とプラスであるのに対して、プラシーボは-2.5となっています。(A参照)またB細胞とナチュラルキラー細胞も天仙液服用グループはでプラスになっており、つまり、天仙液は免疫機能を向上させる効果があるということが言えます。(B参照)また、天仙液は化学治療の副作用を軽減させる効果も確認されました。(C参照)
※本試験に関するデータはアメリカ国立衛生研究所(NIH)の臨床試験公式サイトに掲載されました。
また、2012年1月18日にイギリス補完代替医療学会誌(Evidence-Based Complementary and Alternative Medicine)に掲載されました。